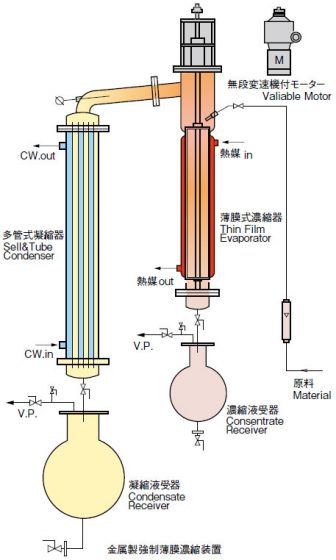
描述
FerroFarRed (Fe2+indicator) 亚铁离子荧光探针
产品标签
FerroFarRed;FeRhoNox-1;FerroOrange;Labile ferrous ion 不稳定铁(II)离子;Fe2+荧光探针;Ferroptosis 铁死亡;C11 BODIPY 581/591 脂质过氧化探针;
产品信息
|
产品名称
|
产品编号 |
规格 |
价格(元) |
|
FerroFarRed (Fe2+ indicator) 亚铁离子荧光探针
|
MX4580-50nmol |
50nmol |
2480
|
| FerroFarRed (Fe2+ indicator) 亚铁离子荧光探针 |
MX4580-100nmol |
100nmol |
4580
|
产品描述
FerroFarRed,也称为SiRhoNox-1、ER-SiRhoNox,是一种特异性检测不稳定的铁(II)离子(Fe2+)的荧光探针。FerroFarRed基本无荧光,一旦与Fe2+反应后,不可逆的生成一种远红荧光产物(Absmax=646nm,FLmax=662nm,图1. FerroFarRed的光谱特征)。生理浓度下的铁(III)离子(Fe3+)或其它除铁离子以外的二价金属离子都不会使其荧光增强(见图2. FerroFarRed的金属离子反应特异性)。FerroFarRed具细胞膜渗透性和高选择性,且在高达100μM的浓度下对细胞几乎无毒性,适用于活细胞内Fe2+的检测,倾向定位在内质网(ER)。适用于荧光显微镜、共聚焦显微镜、荧光酶标仪以及流式细胞仪(配置红色激光器)分析。
图1.FerroFarRed的光谱特征。FerroFarRed在0.05M HEPES buffer,pH 7.4下的吸收光谱(左)和荧光光谱(右)。FerroFarRed的最大吸收波长在646nm,而最大荧光波长在662nm。
图2.FerroFarRed的金属离子反应特异性。FerroFarRed(5 μM)与各种金属离子反应后,用荧光酶标仪测定荧光强度(激发波长:630nm,发射波长665nm)。可见,仅与Fe2+反应后发生显著的荧光增强。
保存与运输方法
保存:≤-20℃避光干燥保存,至少1年有效。
运输:冰袋运输。
注意事项
1) FerroFarRed倾向定位在内质网,但也可能检测细胞质池内的Fe2+,目前针对这一点未做明确评估。
2) 荧光染料均存在淬灭问题,请尽量注意避光,以减缓荧光淬灭。
3) 为了您的安全和健康,请穿实验服并戴一次性手套操作。
使用说明
一、 需要自行准备的材料
1.1 细胞培养级或超纯DMSO(比如:MS4601A-100ML)【强烈建议将高纯的DMSO分装成单次用量保存在极低温冷冻室内,比如-80℃,避免吸潮。降解的DMSO可能会增加FerroFarRed的背景信号】
1.2 合适的观察缓冲液(比如:PBS, pH 7.4;HBSS;等)。不要含酚红。
1.3 无血清细胞培养基(D-MEM等)
二、探针准备
2.1从冰箱取出FerroFarRed,置于室温回温至少30min,将其置于微量离心机内低速离心。将瓶内的粉末离心到管底后,再开盖。
2.2 往一管FerroFarRed(50nmol)内加入50μl 高质量DMSO,用枪反复吹吸5次或以上,使其完全溶解即得到1mM FerroFarRed储存液。【注意:FerroFarRed是蓝色固体,但溶液几乎无色(浅蓝色)】。建议单次用完储存液,若实在用不完,请根据单次用量分装,置于-80℃避光保存。用中性缓冲液来稀释储存液。
三、HeLa细胞Fe2+的染色步骤(荧光成像分析)
3.1 在玻底培养皿内接种细胞,培养过夜。
3.2从培养皿内吸走培养基,用合适的观察缓冲液(比如:HBSS)清洗两次。
3.3 用无血清细胞培养基稀释1mM FerroFarRed储存液,制备成5mM的染色工作液。
3.4 将染色工作液加入培养皿内,于37℃孵育1h。
【注意:①建议根据细胞类型和自身实际需求优化工作浓度和孵育时间。②如果细胞很容易从培养皿上脱落,建议使用多聚L-赖氨酸或其它包被基质包被的培养皿来接种细胞。】
3.5 染色后用观察缓冲液(比如:HBSS)清洗一次,替换成新的观察缓冲液。
3.6 在荧光显微镜下观察细胞。
四、HepG2细胞Fe2+的测定(流式分析)
4.1 于多孔培养板内接种细胞,过夜培养。
4.2 从培养板内吸走培养基,用合适的观察缓冲液(比如:HBSS)轻轻的清洗两次。
4.3 用无血清细胞培养基稀释1mM FerroFarRed储存液,制备成5mM的染色工作液。
4.4 将染色工作液加入培养板内,于37℃孵育1h。
【注意:建议根据细胞类型和自身实际需求优化工作浓度和孵育时间。】
4.5 染色后,用PBS清洗一次,之后加入0.25% 胰酶-EDTA消化细胞。
4.6 于冰上用PBS稀释0.25% 胰酶-EDTA,之后500 x g离心细胞悬液5min,以沉淀细胞。
【注意:不可用血清来中和胰酶。】
4.7 吸走上清,用PBS重悬细胞。
4.8 用细胞筛网(40μm尼龙筛网)过滤细胞,去除细胞碎片。
4.9 上机,流式细胞仪分析。
五、荧光检测
对于激光激发:635nm波长左右的激光器比较适合。荧光在660nm左右观察。
对于荧光显微镜观察:选择检测Cy5的红色激发滤片。对于流式分析,选择检测APC的滤片。
相关产品
| 货号 |
名称 |
规格 |
| MX5211-1MG |
C11 BODIPY 581/591脂质过氧化荧光探针 |
1mg |
| MX4558-50UG |
FeRhoNox-1 (Fe2+indicator)亚铁离子荧光探针 |
50μg |
| MX4559-24UG |
FerroOrange (Fe2+indicator)亚铁离子荧光探针 |
24μg |
| MX4580-50nmol |
FerroFarRed (Fe2+indicator)亚铁离子荧光探针 |
50nmol |
| MX5401-1MG |
MitoPerOx Mitochondrial Lipid Peroxidation Indicator
线粒体脂质过氧化探针 |
1mg |
| MX5402-1MG |
BODIPY 558/568 C12脂质转运荧光探针 |
1mg |
| MS5598-100MG |
Ammonium iron(Ⅱ) sulfate hexahydrate, 99.997% trace metals basis
硫酸亚铁(II)铵,六水合物 |
100mg |
| MS5599-1G |
2,2′-Bipyridyl 2,2′-联吡啶 |
1g |
| MS3501-500ML |
Hanks’ Balanced Salt Solution (w/o Ca2+&Mg2+, w/o phenol red )
Hanks平衡盐溶液(无钙镁,无酚红) |
500ml |
| MS3505-500ML |
1× Hanks’ Balanced Salt Solution (w/Ca2+&Mg2+, w/o phenol red )
1×Hanks平衡盐溶液(含钙镁,无酚红) |
500ml |
FerroFarRed的染色示例(来自文献)
Ref 1. Li Z, Jiang L, Chew SH, et al. Carbonic anhydrase 9 confers resistance to ferroptosis/apoptosis in malignant
mesothelioma under hypoxia. Redox Biology. 2019 Sep;26:101297. DOI: 10.1016/j.redox.2019.101297. PMID:
31442913; PMCID: PMC6831888.
检测方法(Fe(II)的细胞定位):Catalytic Fe(II) was detected with a fluorescent turn-on probe, SiRhoNox-1 (FerroFarRed;), as previously described. Cells (5 × 104) were cultured in normoxia on 35-mm glass bottom dish for 16 h at 37 °C. After treatment with CA9 inhibitors under hypoxia for 48 h, cells were co-stained with 5 μM of SiRhoNox-1 and 200 nM of LysoTracker Green in FluoroBrite DMEM for 30 min at 37 °C in normoxia, followed by incubation with 75 nM of MitoTracker Red for another 30 min. We confirmed that 1-h incubation in FluoroBrite DMEM containing 0.1 mg/L (0.25 μM) Fe(NO3)3 scarcely affects iron metabolism of the cells within this limited period. Medium was replaced with new FluoroBrite DMEM, followed by observation with a confocal microscope (LSM880, Carl Zeiss; Oberkochen, Germany). The excitation/emission used for SiRhoNox-1, LysoTracker and MitoTracker probes were 633/670, 504/511 and 579/599 nm, respectively. Local signal intensity of the regions overlapped with each organelle-trackers were analyzed with ZEN Imaging Software (Carl Zeiss).
Fig. 1 CA9 overexpression in MM cells correlates with increased catalytic Fe(II) in response to hypoxia. (F) Differential levels of catalytic Fe(II) in normoxia or hypoxia of ACC-Meso-1 cells were determined by staining with SiRhoNox-1 (5 μM), followed by evaluation with a flow cytometer after 48 h-incubation. (G) Localization of catalytic Fe(II) in normoxic or hypoxic ACC-Meso-1 cells were analyzed by co-staining of SiRhoNox-1 (5 μM), LysoTracker (200 μM) and MitoTracker (75 μM) after 48 h-incubation and observation with a confocal microscope. Integrated intensity per cell (N =7) was quantified by ZEN Imaging Software (ZEISS) (means ± SEM; *P < 0.05, **P < 0.01, ***P< 0.001 vs each control unless indicated by bar). Refer to text for details. SM, sarcomatoid mesothelioma; EM, epithelioid mesothelioma; N, normoxia; H, hypoxia; A.U., arbitrary unit.